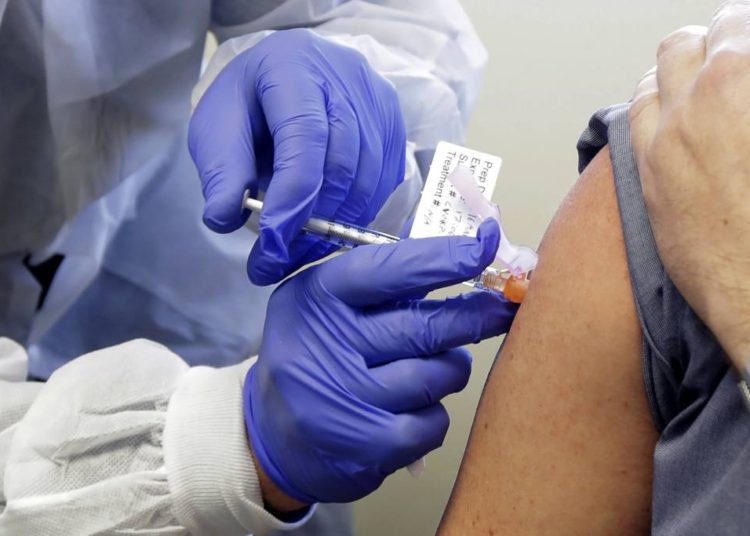
El gobierno de Estados Unidos firmó un contrato con Pfizer para la entrega de 100 millones de dosis de una vacuna contra el COVID-19 que está elaborando la farmacéutica, anunció el miércoles el secretario de Salud, Alex Azar.
Según el acuerdo de suministro, el Gobierno también puede adquirir hasta 500 millones de dosis adicionales.
EE.UU. pagará esta suma a las compañías cuando reciba las dosis, después de que Pfizer fabrique con éxito la vacuna y obtenga la aprobación o autorización para su uso de la Administración de Medicamentos y Alimentos de EE.UU. (FDA, por sus siglas en inglés).
El acceso a la vacuna contra el covid-19 será gratuito para todos los ciudadanos de EE.UU., según el Gobierno.
«Estamos muy satisfechos por haber firmado este importante acuerdo con el Gobierno de EE.UU. para el suministro de los 100 millones de dosis iniciales tras su aprobación, como parte de nuestro compromiso de abordar la amenaza para la salud global. Este acuerdo es uno de los muchos pasos para proporcionar acceso mundial a vacunas seguras y eficaces contra el covid-19. También estamos en conversaciones avanzadas con muchos otros organismos gubernamentales y esperamos anunciar acuerdos de suministro adicionales pronto. Nuestro objetivo sigue siendo proporcionar una vacuna covid-19 segura y efectiva a muchas personas en todo el mundo, lo más rápido posible», ha destacado el director general de BioNTech, Ugur Sahin.
Pruebas positivas en humanos
A primeros de julio las empresas anunciaron que una posible vacuna contra el covid-19 había arrojado resultados positivos durante las primeras pruebas.
Como parte del programa de investigación BNT162, la compañías han creado cuatro vacunas candidatas contra el SARS-CoV-2, siendo la denominada BNT162b1 la que ha mostrado resultados prometedores para neutralizar la proteína usada por el virus para adherirse a la superficie de las células humanas.
Actualmente, cuatro vacunas candidatas contra el covid-19 están en fase de prueba 1/2 en EE.UU. y Alemania, es decir, su seguridad está siendo evaluada, así como la tolerabilidad de los pacientes al medicamento y la inmunogenicidad que produce en distintas dosis.
Los datos adicionales de los ensayos clínicos en curso de fase 1/2 permitirán la selección de un candidato principal y el nivel de dosis para un estudio global de seguridad y eficacia de fase 2b/3, que puede comenzar a finales de este mes y que, de momento, está a la espera de una aprobación reglamentaria.
La vacuna candidata no ha sido aún aprobada para su distribución, pero si los estudios continúan siendo exitosos y recibe el visto bueno de las autoridades competentes, «las empresas esperan fabricar hasta 100 millones de dosis para finales de 2020 y, potencialmente, más de 1.300 millones de dosis para finales de 2021».






EMPEZO EL NEGOCIO MUNDIAL!!!… AHORA LA OMS VA A DESCARTA ESTA VACUNA…